Úvod.
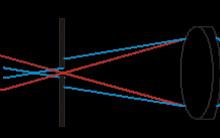
Konfokálny mikroskop sa líši od „klasického“ optického mikroskopu (pozri) tým, že v každom okamihu je zaznamenaný obraz jedného bodu objektu a skenovaním (pohybom vzorky alebo preskupením optického systému) sa vytvorí úplný obraz. . Aby bolo možné registrovať svetlo len z jedného bodu, je za šošovkou objektívu umiestnená malá clona tak, aby svetlo vyžarované analyzovaným bodom (červené lúče na ryža. 1b), prechádza cez clonu a bude zaznamenané, a svetlo zo zostávajúcich bodov (napríklad modré lúče na ryža. 1b) je blokovaný hlavne bránicou. Druhou vlastnosťou je, že iluminátor nevytvára rovnomerné osvetlenie zorného poľa, ale zameriava svetlo na analyzovaný bod. (obr. 1c). To sa dá dosiahnuť umiestnením druhého zaostrovacieho systému za vzorku, ale to si vyžaduje, aby bola vzorka priehľadná. Okrem toho sú šošovky objektívov zvyčajne relatívne drahé, takže použitie druhého zaostrovacieho systému na osvetlenie je málo prospešné. Alternatívou je použitie rozdeľovača lúčov, takže dopadajúce aj odrazené svetlo je zaostrené jednou šošovkou (obr. 1d). Táto schéma tiež uľahčuje nastavenie.
Ryža. 1a. Dráha lúčov v bežnom optickom mikroskope, keď svetlo z rôznych bodov vzorky vstupuje do fotodetektora.

Ryža. 1b. Použitie clony môže výrazne znížiť osvetlenie pozadia z bodov vzorky mimo analyzovanej oblasti.

Ryža. 1. storočie Ďalšie zvýšenie kontrastu sa dosiahne použitím podsvietenia, ktoré zaostrí svetlo na analyzovaný bod.

Ryža. 1 rok Konštrukcia rozdeľovača lúčov zjednodušuje návrh mikroskopu a proces nastavenia pomocou dvojitej šošovky
(na osvetlenie a zber odrazeného signálu).
Rozlíšenie a kontrast v konfokálnom mikroskope.
Uvažujme teraz matematicky, ako a ako kvantitatívne sa mení kontrast pri použití konfokálnej mikroskopie. Po prvé, keďže v r konfokálny mikroskop svetlo prechádza šošovkou dvakrát, funkcia rozmazania bodov (ďalej len PSF, pozri definíciu v) má tvar
Pre kvalitatívne pochopenie je vhodné považovať každý PSF za pravdepodobnosť, že fotón zasiahne bod so súradnicami , alebo že fotón bude zaznamenaný z bodu so súradnicami , potom konfokálne PSF je súčinom nezávislých pravdepodobností. Zapnuté ryža. 2 Je zobrazený obraz bežného PSF a konfokálneho PSF.

Ryža. 2. Konfokálne PSF je zobrazené vpravo a bežné PSF je zobrazené vľavo.
Ak na rozlíšenie použijeme Rayleighovo kritérium (26% pokles od distribučného maxima), zistíme, že rozlíšenie v konfokálnom mikroskope sa zvyšuje, ale nie výrazne. Pre konfokálny mikroskop
kým pre bežný mikroskop
![]()
Hlavnou výhodou konfokálneho mikroskopu však nie je zvýšenie rozlíšenia v zmysle Rayleighovho kritéria, ale výrazné zvýšenie kontrastu. Najmä pre konvenčné PSF v ohniskovej rovine je pomer amplitúdy v prvom laterálnom maxime k amplitúde v strede 2 %, v prípade konfokálneho mikroskopu bude tento pomer 0,04 %. Zapnuté ryža. 3 Tam, kde je to dôležité, je uvedený praktický príklad. V hornej časti obrázku vidíme, že slabý objekt (intenzita je 200-krát menšia ako intenzita jasného objektu) nie je možné detegovať bežným mikroskopom, hoci vzdialenosť medzi objektmi je výrazne väčšia, ako predpisuje Rayleigh. kritérium. Zároveň by mal byť tento objekt dobre zaznamenaný v konfokálnom mikroskope (spodná časť obrázku 3).

Ryža. 3. Rozloženie intenzity pre prípad bežného mikroskopu (horný obrázok) a konfokálneho mikroskopu (dolný obrázok).
Maximálna intenzita slabého objektu je 200-krát menšia ako intenzita jasného [ 1
].
Distribúcia intenzity pozdĺž optickej osi pre konfokálny mikroskop je určená výrazom

Potom pomocou Rayleighovho kritéria získame rozlíšenie pozdĺž optickej osi
![]()
Tu je dôležité poznamenať, že rozlíšenie pozdĺž optickej osi by sa nemalo zamieňať s hĺbkou ostrosti v bežnom mikroskope. Hĺbka ostrosti je zvyčajne stokrát väčšia ako rozlíšenie pozdĺž optickej osi.
Účinok clony v ohniskovej rovine.
Jedným z parametrov, ktorý sa vo vyššie uvedenom popise nijako neobjavil, je veľkosť otvorov v ohniskovej rovine ožarovacích a zberných šošoviek. Všimnite si, že počas analýzy sme mlčky predpokladali, že zdroj je bodový zdroj a za tohto predpokladu sme získali funkciu rozmazania bodu (PSF) pre konvenčný a konfokálny mikroskop. Výsledné PSF popisujú vlastnosti šošovky objektívu a obraz clony v rovine objektu určuje svetlo, z ktorého oblasti sú snímané fotodetektorom. Je však jasné, že zmenšenie veľkosti clony znižuje množstvo prepusteného svetla, zvyšuje úroveň šumu a v konečnom dôsledku môže negovať akékoľvek dosiahnuté zisky kontrastu. Vyvstáva teda otázka optimálneho výberu veľkosti clony a rozumného kompromisu.
Clona s otvorom menším ako Airy spot jednoducho vedie k strate intenzity a nemá žiadny vplyv na rozlíšenie. Veľkosť clony jedného bodu Airy umožňuje maximálne využitie rozlišovacej schopnosti šošovky objektívu. Ako najvhodnejší kompromis sa však javí veľkosť clony približne 3-5 násobok Airy spot. Malo by byť zrejmé, že veľkosť, o ktorej sa tu diskutuje, sa vzťahuje na veľkosť obrazu v rovine objektu, a preto skutočná veľkosť otvoru clony závisí od zväčšenia šošovky. Konkrétne, pri použití 100x šošovky bude clona s 1 mm clonou vyčnievať do roviny objektu do kruhu s polomerom 10 µm.
Aby sa matematicky zohľadnila prítomnosť membrány a skonštruovala sa nová funkcia rozloženia intenzity, je potrebné vykonať konvolúciu
a pre konfokálny mikroskop vynásobte už získanú funkciu číslom . Výsledné rozloženie intenzity pre prípad clony s veľkosťou 5 Airy spotov je znázornené v ryža. 4.

PREHĽAD LITERATÚRY
Intravitálna reflexná konfokálna laserová skenovacia mikroskopia: história vzniku, princíp činnosti, možnosti aplikácie v dermatológii
N.N. LUKASHEVA1, S.B. TKACHENKO1, N.N. POTEKAEV2, T.S. KUZMINA1, E.A. VASILEVSKAYA1
1 Laboratórium na štúdium reparačných procesov v koži, Výskumný ústav molekulárnej medicíny MMA pomenované po. ONI. Sechenov; 2 oddelenie
kožné a pohlavné choroby FPPOV MMA pomenované po. ONI. Sechenov
Doživotná reflexná konfokálna laserová skenovacia mikroskopia: história založenia, princíp fungovania, možnosti využitia v dermatológii
N.N. LUKASHEVA1, S.B. TKACHENKO1, N.N. POTEKAEV2, T.S. KUZ'MINA1, E.A. VASILEVSKAYA1
1 Laboratórium štúdiom reparačných procesov v koži Výskumného ústavu molekulárnej medicíny I.M. Sechenov Moskovská lekárska akadémia; 2 FPPOP spoločnosti I.M. Sechenov Moskovská lekárska akadémia
Jedným z trendov modernej medicíny je využívanie neinvazívnych metód výskumu zachovania orgánov. Vďaka vedeckému vývoju a zavádzaniu inovatívnych technológií do praxe sa v poslednom desaťročí objavili nové neinvazívne metódy s vysokým rozlíšením na štúdium štruktúry kože a iných tkanív. Patria sem optická koherentná tomografia, vysokofrekvenčné ultrazvukové skenovanie, nukleárna magnetická rezonancia a konfokálna laserová skenovacia mikroskopia (CLSM). Posledná uvedená metóda zaujíma osobitné miesto medzi zobrazovacími technológiami, pretože umožňuje získať snímky epidermis a povrchovej dermy s rozlíšením blízkym tradičnej svetelnej mikroskopii.
Základný koncept konfokálnej mikroskopie vyvinul M. Minsky v polovici 50. rokov minulého storočia s cieľom študovať neurónovú sieť v natívnom preparáte mozgového tkaniva bez predchádzajúceho farbenia. Tento vynález zostal nepovšimnutý kvôli tomu, že v tom čase chýbal výkonný svetelný zdroj potrebný na získanie obrazu, ako aj vhodné počítačové vybavenie na spracovanie prijatých informácií. Po M. Minsky v 60. rokoch M. Egger a M. Petran vytvorili viaclúčový konfokálny mikroskop pomocou rotujúceho disku na štúdium nefarbených preparátov mozgového tkaniva a gangliových buniek. V roku 1973 sa vďaka práci M. Eggera na ďalšom zdokonaľovaní konfokálneho laserového skenovacieho mikroskopu,
Klin Dermatol Venerol 2008;5:10-15
boli publikované rozlíšiteľné obrazy buniek získané pomocou tejto metódy. Rozvoj počítačových a laserových technológií v 70. – 80. rokoch minulého storočia, ako aj možnosť získavania digitálnych obrazov viedli k zvýšeniu záujmu o konfokálnu mikroskopiu. A v osemdesiatych rokoch minulého storočia niekoľko skupín výskumníkov demonštrovalo použitie tandemových skenovacích konfokálnych mikroskopov na zobrazenie ľudských a zvieracích tkanív in vivo. Krátko po vypršaní patentu M. Minského využilo niekoľko výskumníkov návrhy konfokálneho laserového skenovacieho mikroskopu na vytvorenie pracovných zariadení. Holandský fyzik G.F. Brakenhoff vyvinul konfokálny rastrovací mikroskop v roku 1979, takmer súčasne s príspevkom C. Shepparda k teórii zobrazovania. T. Wilson, W. Amos a J. White vyvinuli tento koncept a neskôr, v 80. rokoch, preukázali užitočnosť konfokálneho zobrazovania pri štúdiu fluorescenčných biologických vzoriek. Prvé komerčne dostupné zariadenie sa objavilo v roku 1987. V 90. rokoch pokrok v optike a elektronike umožnil vytvoriť výkonnejšie a spoľahlivejšie lasery, vysokoúčinné skenovacie zrkadlové prvky, vysokovýkonnú vláknovú optiku, tenšie vrstvy dielektrického povlaku a detektory, ktoré znížená hlučnosť.charakteristiky . Vďaka vysokorýchlostným počítačovým systémom, ktoré sa objavili koncom 90-tych rokov, zväčšeným monitorom a technológiám, ktoré umožňujú uchovávať veľké množstvo informácií, sa začala nová výbušná etapa vo vývoji CLSM, pokiaľ ide o počet aplikácií, pre ktoré by sa dal použiť. .

zameraný. Prvé správy o použití konfokálneho laserového skenovacieho mikroskopu na in vivo zobrazovanie ľudskej kože boli publikované v roku 1995. Reflexnú konfokálnu mikroskopiu používanú v dermatológii vyvinuli M. Rajadhyaksha et al. a vylepšená "Lucid Inc". V 90. rokoch študovali skupiny výskumníkov (S. Gonzalez et al.) rôzne patologické stavy kože pomocou reflexnej konfokálnej mikroskopie a ukázali veľký význam tejto metódy ako užitočného diagnostického nástroja.
V závislosti od použitého svetelného zdroja existujú rôzne typy konfokálnej mikroskopie. Konfokálna mikroskopia sa môže vykonávať s laserom ako svetelným zdrojom alebo bez neho. Tandemový skenovací konfokálny mikroskop zvyčajne používa ortuťovú lampu. V porovnaní s tandemovým skenovacím konfokálnym mikroskopom využíva CLSM laserový lúč so špecifickou vlnovou dĺžkou a vysokým výkonom osvetlenia. Okrem toho sa rozlišuje medzi fluorescenčným a reflexným CLSM. Pre svoju bezpečnosť a neinvazívnosť je vhodnejšie použiť intravitálny reflexný CLSM.
Základný princíp reflexného CLSM je založený na použití bodového svetelného zdroja (laserového lúča) osvetľujúceho malý bod v tkanive, po ktorom nasleduje zachytenie odrazeného svetla cez opticky spriahnutú apertúru (inklúzia) (obr. 1). . Odrazené svetlo prechádza cez inklúziu, čo spôsobí, že k detektoru sa dostane iba zaostrené svetlo, zatiaľ čo nezaostrené svetlo sa odkloní. Týmto spôsobom sa určí jeden plán v rámci vzorky, ktorý je v centre pozornosti. Numerická apertúra šošovky objektívu, vlnová dĺžka a veľkosť otvorenej apertúry (inklúzie) určujú rozlíšenie obrazu získaného pomocou reflexného CLSM. Ako zdroj svetla pre reflexnú konfokálnu mikroskopiu možno použiť lasery rôznych vlnových dĺžok. Dlhšie blízke infračervené vlnové dĺžky prenikajú hlbšie do pokožky, ale poskytujú nižšie rozlíšenie v porovnaní s kratšími vlnovými dĺžkami vo viditeľnom spektre. K odrazu svetla dochádza v dôsledku lokálnych rozdielov v indexe lomu v tkanive. Pre jednotlivé organely a štruktúry je to spôsobené rozdielom v indexe lomu v porovnaní s bezprostredným prostredím. Melanozómy vykazujú silný odraz pri vlnových dĺžkach vo viditeľnom (400 – 700 nm) a blízkom infračervenom (700 – 1064 nm) spektre v dôsledku ich vysokého indexu lomu v porovnaní s okolitou epidermou. Preto bunky obsahujúce
Ryža. 1. Schéma činnosti konfokálneho laserového rastrovacieho mikroskopu.
melanín, ako sú bazálne keratinocyty a melanocyty, vytvárajú jasný obraz.
Existujú konfokálne skenovacie laserové mikroskopy od rôznych výrobcov: Vivascope 1000, 1500, 2500 Lucid Inc., Rochester, NY; Optiscan F900, Optiscan Pty. Ltd., Notting Hill, VIC, Austrália atď. (obr. 2). Pomocou konfokálneho laserového mikroskopu Vivascope 1500 spoločnosť Lucid Inc. Laserové skenovanie sa vykonáva pri vlnovej dĺžke 830 nm s optickým výkonom maximálne 16 mW, ktorý nespôsobuje poškodenie tkaniva ani poškodenie oka. Objektív poskytuje 30-násobné zväčšenie (NA 0,9) s približne 1 µm laterálnym rozlíšením a 5 µm axiálnym rozlíšením (hrúbka rezu). Mikroskop používa šošovku ponorenú do vody, pretože index lomu vody je blízky indexu lomu epidermy, čo minimalizuje sférickú aberáciu spôsobenú povrchovými vrstvami epidermálnych buniek pri zobrazovaní hlbšie v derme. Skenovanie prebieha v XY rovinách 4x4 mm s veľkosťou rámca 0,5x0,5 mm, frekvenciou 9 snímok za sekundu. Tento systém dokáže zobraziť normálnu kožu v hĺbke 200 až 400 µm, čo je dostatočné na zobrazenie epidermis a hornej dermis (papilárnej a hornej retikulárnej). Program spracuje obraz naskenovaný cez imerznú šošovku Lucid Stable View s rozlíšením 1000×1000 pixelov.
KLINICKÁ DERMATOLÓGIA A VENERELOLÓGIA 5, 2008 |

PREHĽAD LITERATÚRY
Ryža. 2. Konfokálny laserový skenovací mikroskop VivaScope 1500 „Lucid Inc“.
Vivascope Ver.7.0 a prenáša sa na 19′′ farebný monitor s maximálnym rozlíšením 1280×1024 pixelov. Pri použití mikroskopu Vivascope 1500 nie je potrebné používať kontrastné látky. Zobrazovanie je možné vďaka prirodzenému kontrastu a rozdielom v indexe lomu zložiek kože, ako je melanín a keratín. Počas prehrávania obrázkov sa používa špeciálne zariadenie na kontakt s pokožkou na zníženie tvorby artefaktov. Na rozhraní obsahuje vodu alebo gél. Toto zariadenie pozostáva z kovového krúžku, ktorý priľne ku koži pacienta a je spojený s mikroskopom vybaveným magnetom. Toto zariadenie má konkávny tvar na umiestnenie ponorného média.
Metóda CLSM umožňuje získať snímky epidermis a povrchovej dermy s rozlíšením blízkym tradičnej svetelnej mikroskopii. Pomocou tejto metódy je možné získať obrázky nielen kožných príveskov, ale aj rozlíšiť bunky rôznych vrstiev epidermis, vlákna papilárnej vrstvy dermis a posúdiť stav kapilár dermy. Môžete študovať morfológiu rôznych buniek, určiť veľkosť, tvar bunkových a subcelulárnych štruktúr. Hlavný rozdiel medzi CLSM a tradičným histologickým vyšetrením je ten
Výsledné obrazy vrstiev kože sú orientované horizontálne (paralelne) k povrchu kože (en face) a sú to tiež poltónové obrazy. V tomto ohľade môžu vzniknúť ťažkosti pri interpretácii získaných výsledkov a pri porovnávaní snímok získaných pomocou intravitálnych údajov CLSM a klasickej biopsie. Pomocou CLS mikroskopu je možné získať jednotlivé obrazy rezov kože a zaznamenať krátke filmy na demonštráciu dynamických procesov vyskytujúcich sa v koži, ako je prietok krvi.
Hlavnými výhodami intravitálneho CLSM je rýchlosť získania výsledkov vyšetrenia oproti klasickému patohistologickému vyšetreniu, ktoré zahŕňa štádiá excízie malého kúsku tkaniva (biopsia), fixácia, rezanie na tenké vrstvy (rezy), farbenie farbivami a následné vyšetrenie pomocou svetelnej mikroskopie. CLSM nemení tkanivo počas štúdie, ako je to v prípade histologického vyšetrenia v dôsledku získavania rezov a ich farbenia, čím sa minimalizuje výskyt artefaktov. Zákrok je navyše bezbolestný, prebieha bez poškodenia kože a nezanecháva jazvy. Metóda umožňuje vyhodnotiť dynamiku chorôb a tiež umožňuje operovať v reálnom čase (pomocou mikrografickej chirurgie).
Prvé práce o využití CLSM v dermatológii boli spojené so získavaním konfokálnych snímok štruktúry zdravej kože a ich následnou analýzou. V prácach M. Rajadhyaksha, S. Gonzalez et al. , M. Huzaira a kol. , K.J. Busam a kol. Poskytujú sa podrobné popisy konfokálnych snímok jednotlivých vrstiev epidermis, dermis, vaskulatúry a kožných príveskov (jednotlivé mazové žľazy, pilosebaceózne folikuly, potné kanáliky). Okrem kvalitatívnych charakteristík sa uvádza morfometrické posúdenie veľkosti buniek, hĺbky umiestnenia a hrúbky vrstiev epidermis, posúdenie jednotlivých vlákien a zväzkov kolagénu v papilárnej a hornej časti retikulárnej dermis, udáva sa priemer lúmenov kapilár, ako aj veľkosti jednotlivých krviniek v lúmenoch vlásočníc. K.J. Busam a kol. T. Yamashita a kol. vo svojich článkoch uvádzajú kvalitatívne hodnotenie melanocytov, uvádzajú morfologické charakteristiky melanocytov, pigmentovaných keratinocytov, melanofágov, umožňujúce
KLINICKÁ DERMATOLÓGIA A VENERELOLÓGIA 5, 2008 |

schopný rozlíšiť tieto bunky v obrazoch získaných intravitálnym CLSM. Množstvo prezentovaných prác hodnotí topografické znaky štruktúry zdravej kože, analyzuje zmeny kože súvisiace s vekom a vplyv slnečného žiarenia na štruktúru epidermis a dermis zdravých ľudí. Pochopenie toho, ako vyzerajú obrazy zdravej epidermy a dermy, je dôležité pre neskoršiu identifikáciu patologických zmien na koži.
Veľké množstvo melanínu prítomného v melanocytových ložiskách robí pigmentované kožné novotvary (névy, melanóm) ideálne na zobrazovanie a diagnostiku pomocou intravitálneho CLSM. Cieľom každej zobrazovacej metódy používanej v dermatológii je diagnostikovať melanóm v skorých štádiách ochorenia, keďže od toho závisí účinnosť terapie. Výsledky výskumu K.J. Busam a kol. , G. Pellacani a kol. R. Langley a kol. , A. Gerger a kol. ukázali, že melanóm sa dá celkom úspešne diagnostikovať pomocou metódy CLSM. Prítomnosť pleomorfných svetlých buniek v epidermis a dermis, ktoré môžu mať tvar hviezdy, majú veľké vetviace procesy a excentricky umiestnené veľké jadrá, ako aj narušenie architektoniky tŕňovej vrstvy v dôsledku nejasných hraníc buniek a svetlosivých častíc (pravdepodobne melanín) distribuovaný v epiderme, umožňuje diagnostikovať melanóm. Intraepidermálny melanóm môže byť tiež diagnostikovaný pomocou tejto metódy na základe kritérií používaných v tradičnej histológii. Konfokálne zobrazenie intraepidermálnych melanómov odhalilo zvýšený počet intradermálnych zväčšených (atypických) melanocytov v solitérnych jednotkách vo všetkých vrstvách epidermis, vrátane horných zrnitých a spinóznych vrstiev. Je potrebné upozorniť, že niektoré príznaky melanómov možno identifikovať aj u nepigmentovaných melanómov. Treba však poznamenať, že malé veľkosti vzoriek, na ktorých boli štúdie vykonané, nám zatiaľ neumožňujú posúdiť citlivosť a špecifickosť prezentovaných kritérií pre konfokálne obrazy pri diagnostike melanómu.
K.J. Busam a kol., R. Langley a kol. naznačujú také znaky melanocytových névov na konfokálnych obrazoch, ako je prítomnosť malých monomorfných okrúhlych alebo oválnych, vysoko lámavých buniek s centrálne umiestnenými jadrami. Tieto bunky môžu byť viditeľné v epiderme, na dermoepidermálnom spojení, typicky okolo dermálnej papily, a v povrchovej derme v závislosti od typu nevusu.
Často sú zoskupené do okrúhlych zhlukov (hniezd) obsahujúcich niekoľko buniek umiestnených v blízkosti krvných ciev. Architektúra rohovej, zrnitej, tŕňovej a bazálnej vrstvy zostáva nezmenená. Dysplastické névy sú charakterizované lokalizovanou redukciou hraníc interakcie medzi keratinocytmi v dermoepidermálnom spojení, prítomnosťou charakteristických pestrofarebných granúl v epiderme (pravdepodobne melanínové telieska) a veľkou rozmanitosťou vo veľkosti a tvare nevomelanocytov, aj keď majú stále tendenciu byť skôr okrúhle alebo oválne ako rozvetvené. Vyššie uvedené štúdie naznačujú, že príznaky melanocytových névov dobre korelujú s tradičným histologickým obrazom. Zostáva však neznáme, či je možné touto metódou presne určiť malígne bunky s malým množstvom pigmentu. Na objasnenie tohto problému je potrebný ďalší výskum.
Intravitálna metóda CLSM umožňuje identifikovať atypické oblasti podozrivé z neoplastických ložísk. V analyzovanej literatúre práce venované štúdiu aktinickej keratózy patria D. Aghassimu a kol. , štúdium spinocelulárneho karcinómu - M. Horn et al. , štúdium bazocelulárneho karcinómu - M. Goldgrier et al. , A.L. Agero a kol. , S. Nori a kol. K. Sauermann a kol. . CLSM umožňuje určiť hranice lézie pred začiatkom terapie, čo môže byť užitočné pri hodnotení hraníc nádorov s radiálnym rastovým vzorcom, vrátane malígneho lentigo melanómu, niektorých bazocelulárnych karcinómov alebo ťažko klinicky diagnostikovaných nádorov. vyšetrovať, ako sú sklerotizujúce infiltratívne bazocelulárne karcinómy. Kľúčové histopatologické znaky aktinickej keratózy zistenej pomocou CLSM zahŕňajú architektonickú poruchu, zväčšené epidermálne jadrá s pleomorfizmom a parakeratózu vedúcu k organizovanej poruche. V súčasnosti je hĺbka prieniku lasera hlavným obmedzením CLSM na diagnostiku aktinickej keratózy. Konfokálnymi znakmi bazocelulárneho karcinómu, najbežnejšieho ľudského kožného nádoru, sú ostrovčeky predĺžených monomorfných nádorových buniek s charakteristickými predĺženými jadrami orientovanými pozdĺž rovnakej osi. Tento vzor rovnomerne orientovaných buniek sa rozprestiera po celej hrúbke epidermis, pričom stráca normálny voštinový vzor a architektúru dermálnych papíl. Hojné krvné cievy vykazujúce nadmernú tortuozitu, ako aj prevažne mononukleárny zápalový infiltrát, sú zmiešané s bunkami bazocelulárneho karcinómu alebo sú s nimi blízko umiestnené
KLINICKÁ DERMATOLÓGIA A VENERELOLÓGIA 5, 2008 |

PREHĽAD LITERATÚRY
Výsledky S. Nori a kol. Veľká retrospektívna multicentrická štúdia ukázala významnú presnosť znakov zistených pomocou CLSM na diagnostiku bazocelulárneho karcinómu in vivo. CLSM teda umožňuje v reálnom čase určiť prítomnosť reziduálneho alebo klinicky sporného bazaliómu. Podľa viacerých štúdií pomáha CLSM pri rýchlom hodnotení hraníc nádoru počas mikrografickej operácie pri vyšetrovaní excíznych preparátov počas operácie. Medzi limitujúce faktory pri použití intravitálneho CLSM na diagnostiku kožných nádorov v súčasnosti patrí okrem iného obmedzená hĺbka vyšetrenia, ktorá bráni presnému zobrazeniu pod povrchovou dermis, a prítomnosť refrakčných vlastností zápalových buniek.
Práca vykonaná v 90. rokoch mnohými výskumníkmi (S. Gonzalez a ďalší) na štúdium rôznych zápalových stavov kože pomocou reflexnej konfokálnej mikroskopie odhalila veľký význam tejto metódy ako užitočného diagnostického nástroja. Najväčšou výhodou metódy je, že umožňuje hodnotenie dynamických procesov pri zápalových ochoreniach kože v reálnom čase a čo je veľmi dôležité, hodnotenie účinnosti terapie dermatóz. Pomocou intravitálneho CLSM sa hodnotili zápalové zmeny pri psoriáze, alergickej a jednoduchej kontaktnej dermatitíde, folikulitíde, lišajoch, bradaviciach, herpes simplex a systémovej skleróze. Na konfokálnych snímkach príznaky psoriasis vulgaris v stacionárnom štádiu zodpovedajú obvyklému histologickému obrazu a zahŕňajú parakeratózu, Munro mikroabscesy, akantózu, dilatáciu kapilár, papilomatózu. Hranice zápalového zamerania sú jasne viditeľné. Pomocou CLSM sú v reálnom čase vizualizované typické príznaky kontaktnej dermatitídy ako spongióza, tvorba mikrovezikúl, zápalový infiltrát a miestami aj epidermálna nekróza. Pomocou tejto metódy sa preukázali patohistologické znaky jednoduchej a alergickej dermatitídy a tiež sa ukázalo, že konfokálna mikroskopia môže byť použitá na posúdenie rasových (u predstaviteľov negroidnej a kaukazskej rasy) znakov akútnej kontaktnej dermatitídy. Konfokálna laserová skenovacia mikroskopia umožňuje rýchlu detekciu vetiev hýf a zápalového infiltrátu v reálnom čase in vivo alebo iv vitro z nechtových platničiek a kúskov kože. Folikulitída zobrazená pomocou konfokálnej mikroskopie môže byť definitívne diagnostikovaná
van priamou demonštráciou intraepidermálnych pustúl, zápalového infiltrátu, spongiózy a dilatácie kapilár. Bradavice na konfokálnych obrazoch sú charakterizované hyperkeratotickým stratum corneum a prítomnosťou viacerých vysoko refrakčných okrúhlych štruktúr s rozmermi 20-40 μm vo vnútri lézie, čo umožňuje rýchlu a definitívnu diagnostiku. Herpetické kožné infekcie zodpovedajú pleomorfným balónikovým keratinocytom a mnohojadrovým obrovským bunkám vo voľnom spojení s keratinocytmi a zápalovými bunkami.
Intravitálna metóda CLSM teda umožňuje in vivo hodnotenie patomorfologických zmien na koži pri rôznych dermatózach, vrátane neoplastických lézií, melanocytových névov, melanómov, čo nepochybne potvrdzuje užitočnosť tohto nástroja v diagnostike rôznych dermatologických ochorení. Vzhľadom na neinvazívnu povahu metódy, možnosť opakovaných viacnásobných štúdií tých istých lézií sa zdá, že CLSM je užitočnejší pri hodnotení dynamických zmien vyskytujúcich sa v koži počas vývoja chorôb a na pozadí prebiehajúcej terapie dermatózy.
Napriek zjavným výhodným aspektom intravitálneho CLSM existujú aj určité obmedzenia a ťažkosti pri používaní tejto metódy. Súčasná technika je zložitá a drahá, a preto nie je široko dostupná pre výskumníkov a lekárov. Niekoľko skupín vedcov v inštitúciách a priemysle však vyvíja jednoduchšie a lacnejšie skenovacie technológie. V porovnaní so súčasnými existujúcimi zariadeniami sa vyvíja aj viac prenosných zariadení, pretože použitie objemných jednotiek je nepohodlné pri skúmaní ťažko dostupných oblastí tela. Limitujúcim faktorom pri použití intravitálneho CLSM je obmedzená hĺbka vyšetrenia, ktorá bráni získaniu presných obrazov pod povrchovou dermis. Pokračuje práca na vytváraní vertikálne orientovaných rezov, ktoré by boli podobné tým, ktoré vidíme pri histologickom vyšetrení, pretože by sa tým výrazne zvýšili možnosti intravitálneho CLSM. Veľkým vedeckým problémom je interpretácia obrazov
Schopnosť čítať, interpretovať a analyzovať konfokálne snímky na zvýraznenie užitočných klinických a histologických informácií. Niekoľko tímov po celom svete vykonáva podrobné štúdie na charakterizáciu konfokálnych snímok a ich koreláciu s histológiou. Jedným z dôležitých problémov zostáva určenie citlivosti a špecifickosti tejto výskumnej metódy v diagnostike rôznych dermatóz.
KLINICKÁ DERMATOLÓGIA A VENERELOLÓGIA 5, 2008 |

LITERATÚRA
1. Abramovits W., Stevenson L.C. Meniace sa paradigmy v dermatológii: nové spôsoby vyšetrenia kože pomocou neinvazívnych zobrazovacích metód. Dermatologické kliniky 2003; 21: 353-358.
2. Minsky M. Mikroskopický prístroj. US patent 1961; 467.
3. Minsky M. Memoir o vynájdení konfokálnej skenovacej mikroskopie. Scanning 1988; 10: 128-138.
4. Egger M.D., Petran M. Nový mikroskop s odrazeným svetlom na prezeranie nezafarbených mozgových a gangliových buniek. Science 1967; 157: 305-307.
5. Davidovits P., Egger M.D. Fotomikrografia endotelových buniek rohovky in vivo. Nature 1973; 244: 366-367.
6. Amos W.B., White J.G. Ako konfokálny laserový skenovací mikroskop vstúpil do biologického výskumu. Biológia bunky 2003; 95: 335-342.
7. Brakenhoff G.J., Blom P., Barends P.Konfokálna skenovacia svetelná mikroskopia s imerznými šošovkami s vysokou apertúrou. J Microscopy 1979; 117: 219-232.
8. Sheppard C.J.R., Wilson T. Vplyv sférickej aberácie na zobrazovacie vlastnosti skenovacích optických mikroskopov. Aplikovaná optika 1979; 18:1058.
9. Hamilton D.K., Wilson T. Skenovacia optická mikroskopia objektívom. Scanning, Journal of Physics E: Scientific Instruments 1986; 19: 52-54.
10. Pawley J.B. Príručka biologickej konfokálnej mikroskopie. New York: Plénum Press 1995.
11. Gonzalez S., Swindells K., Rajadhyaksha M., Torres A.Meniace sa paradigmy v dermatológii: konfokálna mikroskopia v klinickej a chirurgickej dermatológii. Clin Derm 2003; 21: 359-369.
12. Rajadhyaksha M., Grossman M., Esterowitz D. a kol.In vivo konfokálna skenovacia laserová mikroskopia ľudskej kože: melanín poskytuje silný kontrast. J Invest Dermatol 1995; 104: 946-952.
13. Rajadhyaksha M., Gonzalez S., Zavislan J.M. Syn R.R. a kol.In vivo konfokálna skenovacia laserová mikroskopia ľudskej kože II: pokroky v prístrojovom vybavení a porovnanie s histológiou. J Invest Dermatol 1999; 113: 101-112.
14. Snímky tkaniva z konfokálneho laserového mikroskopu in vivo. Laser Focus World 1997; 33: 119-127.
15. Rajadhyaksha M., Zavislan J.M. Konfokálna reflexná mikroskopia nezafarbeného tkaniva in vivo. Retinoids 1998; 14:26-30.
16. Gonzalez S., Rajadhyaksha M., Anderson R.R. Neinvazívne (v reálnom čase) zobrazovanie histologického okraja proliferatívnej kožnej lézie in vivo. J Invest Dermatol 1998; 111: 538-539.
17. Gonzalez S., Gonzalez E., White W.M. a kol.Alergická kontaktná dermatitída: korelácia in vivo konfokálneho zobrazovania s rutinnou histológiou. J Am Acad Dermatol 1999; 40: 708-713.
18. Swindle L.D., Thomas S.G., Freeman M., Delaneyz P.M.Pohľad na normálnu ľudskú pokožku in vivo pozorovaný pomocou fluorescencie optické konfokálne vlákna
mikroskopické zobrazovanie. J Invest Dermatol 2003; 121: 706-712.
19. Delaney P.M., Harris M.R., Kráľ R.G.Nová mikroskopia využívajúca konfokálne zobrazovanie z optických vlákien a jej vhodnosť na zobrazovanie podpovrchových krvných ciev in vivo. Clin Exp Pharmacol Physiol 1993; 197:20.
20. Busam K.J., Charles C., Lohmann C.M. a kol.Detekcia intraepidermálneho malígneho melanómu in vivo pomocou konfokálnej skenovacej laserovej mikroskopie. Melanómový výskum 2002; 12: 349-355.
21. Aghassi D., Anderson R.R., González S.Konfokálne laserové mikroskopické zobrazovanie aktinických keratóz in vivo: predbežná správa. J Am Acad Dermatol 2000; 43: 42-48.
22. Používateľská príručka VivaScope 1500 Lucid Inc.
23. Corcuff P., Bertrand C., Leveque J.L.Morfometria ľudskej epidermy in vivo pomocou reálny čas konfokálna, mikroskopia. Arch Dermatol Res 1993; 285: 475-481.
24. Meyer L.E., Otberg N., Richter H., Sterry W. a kol. Nové vyhliadky v dermatológii: na báze vlákniny konfokálna skenovacia laserová mikroskopia. Laserová fyzika 2006; 16:5: 758-764.
25. Serup J., Jemec G.B.E., Grove G.L. Príručka neinvazívnej techniky metódy a pleť. 2. vyd. CRC Press 2006; 32: 267-276.
26. Huzaira M., Rius F., Rajadhyaksha M., Anderson R.R. a kol.Topografické variácie v normálnej koži, ako sú pozorované in vivo reflexnou konfokálnou mikroskopiou. J Invest Dermatol 2001; 116: 846-852.
27. Busam K.J., Charles C., Lee G., Halpern A.C.Morfologické znaky melanocytov, pigmentovaných keratinocytov a melanofágov in vivo
konfokálna skenovacia laserová mikroskopia. Mod Pathol 2001; 14: 9: 862-868.
28. Yamashita T., Kuwahara T., Gonzalez S., Takahashi M. Neinvazívne vizualizácia melanínu a melanocytov pomocou odrazový režim konfokálna mikroskopia. J Invest Dermatol 2005; 124: 235-240.
29. Sauermann K., Clemann S., Jaspers S., Gambichler T. a kol.Zmeny súvisiace s vekom ľudskej kože skúmané histometrickými meraniami pomocou konfokálnej laserovej skenovacej mikroskopie in vivo. Výskum a technológia pleti 2002; 8: 52-56.
30. Sauermann K., Jaspers S., Koop U., Wenck H.Lokálne aplikovaný vitamín C zvyšuje hustotu dermálnych papíl u starnúcej ľudskej kože. BMC Dermatology 2004; 4:13 doi:10.1186/1471-5945-4-13.
31. Pellacani G., Cesinaro A.M., Seidenari S. Odrazový režim konfokálna mikroskopia pigmentovanej kože lézie-zlepšenie v špecifickosti diagnostiky melanómu. J Am Acad Dermatol 2005; 53: 979-985.
32. Langley R.G.B., Rajadhyaksha M., Dwyer P.J., Sober A.J. a kol.Konfokálna skenovacia laserová mikroskopia benígnych a malígnych melanocytových kožných lézií in vivo. J Am Acad Dermatol 2001; 45: 365-376.
33. Gerger A., Koller S., Kern T., Massone C. a kol.Diagnostická použiteľnosť in vivo konfokálnej laserovej skenovacej mikroskopie v melanocytových kožných nádoroch. J Invest Dermatol 2005; 124: 493-498.
34. Busam K.J., Hester K., Charles C. a kol.Detekcia klinicky amelanotického malígneho melanómu a hodnotenie jeho okrajov in vivo konfokálnou skenovacou laserovou mikroskopiou. Arch Dermatol 2001; 137: 923-929.
35. Horn M., Gerger A., Koller S. a kol. Použitie konfokálneho laserového skenovania mikroskopia v mikrochirurgii pre invazívny skvamocelulárny karcinóm. British Journal of Dermatology 2007; 156: 81-84.
36. Goldgrier M., Fox C.A., Zavislan J.M. a kol.Neinvazívne zobrazovanie, liečba a mikroskopické potvrdenie klírensu bazocelulárneho karcinómu. Dermatol Surg 2003; 29: 205-210.
37. Agero A.L.C., Busam K.J., Benvenuto-Andrade C. Reflexná konfokálna mikroskopia pigmentovaného bazocelulárneho karcinómu. J Am Acad Dermatol 2006; 54: 638-643.
38. Nori S., Rius-Dıaz F., Cuevas J. a kol. Citlivosť a špecifickosť odrazový režim konfokálna mikroskopia na diagnostiku bazocelulárneho karcinómu in vivo: multicentrická štúdia. J Am Acad Dermatol 2004; 51: 923-930.
39. Sauermann K., Gambichler T., Wilmert M. a kol.Vyšetrovanie bazocelulárneho karcinómu konfokálnou laserovou skenovacou mikroskopiou in vivo. Výskum a technológia pleti 2002; 8: 141-147.
40. Gonzalez S., Sackstein R., Anderson R.R., Rajadhyaksha M. Reálny čas dôkaz prenosu leukocytov in vivo v ľudskej koži pomocou reflexnej konfokálnej mikroskopie. J Invest Dermatol 2001; 117:2: 384-386.
41. González S., Rajadhyaksha M., Rubinstein G., Anderson R.R.
Charakterizácia psoriázy in vivo pomocou reflexnej konfokálnej mikroskopie. J Med 1999; 30: 337-356.
42. Astner S., Gonzalez E., Cheung A.C. a kol. Neinvazívne hodnotenie kinetiky alergickej a dráždivej kontaktnej dermatitídy. J Invest Dermatol 2005; 124: 351-359.
43. Hicks S.P., Swindells K.J., Middelkamp-Hup M.A. a kol. Konfokálna histopatológia dráždivej kontaktnej dermatitídy in vivo a vplyv farby kože (čierna vs. biela). J Am Acad Dermatol 2003; 48: 727-734.
44. Gonzalez S., Rajadhyaksha M., Gonzalez-Serva A. a kol. Konfokálne odrazové zobrazovanie folikulitídy in vivo: korelácia s rutinnou histológiou. J Cutan Pathol 1999; 26: 201-205.
45. Markus R., Huzaira M., Anderson R.R., Gonzalez S.Lepší prípravok hydroxidu draselného? In vivo diagnostika tinea pomocou konfokálnej mikroskopie. Arch Dermatol 2001; 137: 1076-1078.
46. Hongcharu W., Dwyer P., Gonzalez S., Anderson R.R.Potvrdenie onychomykózy in vivo konfokálnou mikroskopiou. J Am Acad Dermatol 2000; 42: 214-216.
47. Goldgeier M., Fox C.A., Muhlbauer J.E.Okamžitá neinvazívna diagnostika herpesvírusu pomocou konfokálnej skenovacej laserovej mikroskopie. J Am Acad Dermatol 2002; 46: 783-785.
48. Sauermann K., Gambichler T., Jaspers S. a kol.Histometrické údaje získané in vivo konfokálnou laserovou skenovacou mikroskopiou u pacientov so systémovou sklerózou. BMC Dermatology 2002; 2:8.
KLINICKÁ DERMATOLÓGIA A VENERELOLÓGIA 5, 2008 |
Margolin 389 p.
Optická mikroskopia využívala všetky výdobytky tak techniky a techniky, ako aj informačných a počítačových technológií. To viedlo k výraznému zlepšeniu existujúcich zariadení a metód na ich použitie, čo následne viedlo k vzniku nových metód, najmä konfokálnej mikroskopie. Konfokálny mikroskop sa líši od klasického optického mikroskopu tým, že v každom okamihu je zaznamenaný obraz jedného bodu objektu a skenovaním (pohybom vzorky alebo preskupením optického systému) sa vytvorí úplný obraz. Princíp rastrovacej elektrónovej mikroskopie je teda implementovaný v unikátnej forme, ktorá umožňuje zaznamenávať a spracovávať signál z každého jednotlivého bodu tak dlho, ako si želáte.
V klasickom mikroskope svetlo z rôznych bodov vzorky vstupuje do fotodetektora. V konfokálnom mikroskope, aby sa zaznamenalo svetlo iba z jedného bodu, sa za šošovku objektívu umiestni malá clona tak, že svetlo vyžarované analyzovaným bodom prechádza clonou a bude sa zaznamenávať a svetlo z analyzovaného bodu zostávajúce body sú blokované hlavne membránou, ako je znázornené na obr. 7.28.
Ryža. 7.28. Schéma prenosu lúča v konfokálnom optickom mikroskope
Ďalšou vlastnosťou je, že iluminátor nevytvára rovnomerné osvetlenie zorného poľa, ale sústreďuje svetlo na analyzovaný bod. To sa dá dosiahnuť umiestnením druhého zaostrovacieho systému za vzorku, ale to si vyžaduje, aby bola vzorka priehľadná. Okrem toho sú šošovky objektívov zvyčajne drahé, takže použitie druhého zaostrovacieho systému na osvetlenie je málo výhodné. Alternatívou je použitie rozdeľovača lúčov, takže dopadajúce aj odrazené svetlo je zaostrené jednou šošovkou. Táto schéma tiež uľahčuje nastavenie.
Uvažujme teraz, ako a ako kvantitatívne sa mení kontrast pri použití konfokálnej mikroskopie. Keďže svetlo v konfokálnom mikroskope prechádza šošovkou dvakrát, funkcia rozostrenia bodu (ďalej označovaná ako PSF) bude výsledkom nezávislých pravdepodobností, že fotón zasiahne bod so svojimi súradnicami alebo že z tohto bodu bude detegovaný fotón.
Ak na rozlíšenie použijeme Rayleighovo kritérium, ukáže sa, že rozlíšenie v konfokálnom mikroskope sa zvýši, ale nie výrazne. Pre konfokálny mikroskop máme výraz pre rozlíšenie r:
Zatiaľ čo pre bežný mikroskop:

Hlavnou výhodou konfokálneho mikroskopu však nie je zvýšenie rozlíšenia v zmysle Rayleighovho kritéria, ale výrazné zvýšenie kontrastu. Najmä pre konvenčné PSF v ohniskovej rovine je pomer amplitúdy na prvom bočnom maxime k amplitúde v strede 2 % a pre konfokálny mikroskop bude tento pomer 0,04 %. Z toho vyplýva, že slabý objekt s intenzitou, napríklad 200-krát menšou ako jasný objekt, nie je možné detekovať bežným mikroskopom, hoci vzdialenosť medzi objektmi môže byť výrazne väčšia ako vzdialenosť predpísaná Rayleighovým kritériom. . Zároveň by mal byť takýto objekt dobre zaznamenaný v konfokálnom mikroskope.
Dôležitým parametrom je veľkosť otvorov v ohniskovej rovine ožarovacích a zberných šošoviek. Obraz otvoru v rovine objektu určuje, z ktorých oblastí je svetlo detegované fotodetektorom. Je zrejmé, že zmenšenie veľkosti otvoru vedie k zníženiu množstva prenášaného svetla, zvyšuje hladinu šumu a v konečnom dôsledku môže negovať akékoľvek dosiahnuté výhody kontrastu. Vyvstáva teda otázka optimálneho výberu veľkosti clony a rozumného kompromisu.
Clona s veľkosťou otvoru menšou ako je bod Airy jednoducho vedie k strate intenzity a nemá žiadny vplyv na rozlíšenie. Jednobodová Airy clona umožňuje maximálne využitie rozlišovacej schopnosti šošovky objektívu. Ako najvhodnejší kompromis sa však javí bránica s veľkosťou otvoru približne 3 až 5-krát väčšou ako Airy spot. Malo by byť zrejmé, že veľkosť, o ktorej sa tu diskutuje, sa vzťahuje na veľkosť obrazu v rovine objektu, a preto skutočná veľkosť otvoru clony závisí od zväčšenia šošovky. Konkrétne, pri použití 100x šošovky bude clona s 1 mm clonou vyčnievať do roviny objektu do kruhu s polomerom 10 µm.
Vývojom myšlienky konfokálnej mikroskopie bol vývoj konfokálneho laserového skenovacieho mikroskopu (KJICM), ktorý bol spôsobený potrebou citlivejších a metrologicky prísnejších metód analýzy tvaru a priestorovej štruktúry pozorovaných objektov. Schematický diagram CLSM s hlavnými funkčnými zapojeniami je znázornený na obr. 7.29.
Hlavnou črtou CLSM je možnosť vrstvenia skúmaného objektu s vysokým rozlíšením a nízkou úrovňou šumu. Dosahuje sa to postupným skenovaním objektu sústredeným lúčom svetla z koherentného zdroja alebo posúvaním stolíka pomocou špeciálnych fluorescenčných sond a špeciálnych metód na obmedzenie svetelných tokov.

Ryža. 7.29. Bloková schéma KJICM:
1 - skenovací stôl; 2 - skúšobná vzorka; 3, 6 - šošovky; 4 - skenovacie zariadenie; 5 - doska na rozdeľovanie lúčov; 7, 9 - ihlové membrány; 8 - prijímač žiarenia; 10 - laser; 11 - riadiaci blok; 12 - počítač; 13 - osový skenovací pohon z.
Použitie dierkovej clony v CLSM, ktorej rozmery sú koordinované so zväčšením mikroskopu a vlnovou dĺžkou, umožňuje zvýšiť rozlíšenie o viac ako 10 %. Je zrejmé, že rozlišovacia schopnosť CLSM a teda aj možnosti analýzy jemných štruktúr môžu v podmienkach skenovania vzorky tenkým lúčom prekročiť podobné možnosti bežného mikroskopu o maximálne 40 %. Rozlíšenie KLCM závisí od metódy mikroskopu a osvetlenia. Stanoví sa rozlíšenie KLCM ako optický systém, tak aj elektronická dráha spracovávanie informácií. Preto pri návrhu KLCM musia byť koordinované jeho obvody, parametre ako rozlíšenie optického systému, krok skenovania, charakteristiky detektora a musia byť zvolené optimálne algoritmy spracovania a vhodný softvér.
Vo všeobecnosti hĺbka poľa KLCM závisí od clony, vlnovej dĺžky, koherencie svetelných zdrojov a veľkosti kolíkovej clony. Ihlová membrána je hlavným dizajnovým prvkom, ktorý odlišuje KLCM od iných typov mikroskopov. Ihlové clony sú navrhnuté tak, aby vytvorili podmienky pre maximálnu alebo úplnú filtráciu svetla vstupujúceho do roviny tvorby obrazu z bodov, ktoré sa nezhodujú s ohniskovou rovinou alebo sa nachádzajú vedľa analyzovaného prvku objektu v ohniskovej rovine.
Výber optimálneho priemeru membrány ihly je dôležitý na získanie požadovaných charakteristík zariadenia. Vzťahy na odhad laterálneho rozlíšenia a hĺbky poľa KJICM sa získajú za predpokladu, že ihlová clona má malý otvor, čo je svetelný bod. V skutočnosti je veľkosť ihlovej membrány konečná a závisí od nej priečne rozlíšenie zariadenia a jas osvetlených prvkov vzorky, posunutý vzhľadom na ohniskovú rovinu pozdĺž osi. z, a hĺbka ostrosti. Pri malých priemeroch ihlovej clony sa svetelný tok zníži, čo znižuje pomer signálu k šumu a znižuje kontrast. Pri väčších priemeroch sa účinnosť ihlovej membrány znižuje zmenšením otvoru.
Konfokálna mikroskopia je jednou z metód optickej mikroskopie, ktorá má výrazný kontrast v porovnaní s bežnými klasickými mikroskopmi. Charakteristickým rysom tejto metódy je použitie membrány, ktorá dokáže prerušiť tok rozptýleného svetla na pozadí.
V konfokálnom mikroskope sa v každom okamihu zaznamenáva obraz jedného prúdu objektu. Kompletný obraz sa získa skenovaním pohybu vzorky alebo preskupením optického systému. Za šošovkou objektívu je umiestnená malá clona tak, že svetlo vyžarované skúmaným bodom ňou prechádza a zaznamenáva sa a svetlo vychádzajúce z iných bodov je clonou oneskorené.
Opísaná metóda výskumu umožňuje študovať vnútornú štruktúru rôznych buniek. S jeho pomocou môžete identifikovať jednotlivé molekuly a bunkové štruktúry, mikroorganizmy, ako aj dynamické procesy prebiehajúce v bunkách.
Popis metódy konfokálnej mikroskopie
Vďaka konfokálnej fluorescenčnej mikroskopii bolo možné získať trojrozmernú submikrónovú expanziu objektov a výrazne sa rozšírila aj schopnosť vykonávať nedeštruktívnu analýzu priehľadných vzoriek. Vďaka použitiu laserov ako svetelných zdrojov v týchto mikroskopoch sa dosahuje zvýšenie ich rozlišovacej schopnosti.
V porovnaní s xenónovými alebo ortuťovými výbojkami majú lasery významné výhody, pretože majú schopnosť byť monochromatické, ako aj vysoko paralelné s vyžarovaným svetelným lúčom. Takéto vlastnosti laserového žiarenia poskytujú optickému systému efektívnejšiu prevádzku, ako aj znižujú množstvo oslnenia a zvyšujú presnosť zaostrenia svetelného lúča.
Na skúmanej vzorke laser neosvetľuje celé zorné pole, ale je zaostrený na určitý bod. Konfokálna clona vám umožní zbaviť sa rozostrenej fluorescencie, pri zmene priemeru clony môžete presne určiť hrúbku optickej vrstvy v blízkosti ohniska laserového lúča. Vďaka tejto vlastnosti umožňuje konfokálna mikroskopia zlepšené rozlíšenie pozdĺž osi Z.
Špeciálne programy, ktorými sú konfokálne mikroskopy vybavené, umožňujú vytvárať trojrozmerné obrazy predmetov zo série optických rezov, ako aj prezerať si ich z rôznych uhlov pohľadu.
Použitie multispektrálneho laserového skenovacieho konfokálneho mikroskopu umožňuje študovať kokolizáciu rôznych látok v bunkách. Multispektrálny režim vám umožňuje vykonávať štúdie FISH pomocou konfokálneho mikroskopu.
Príklady štúdií uskutočnených pomocou konfokálneho mikroskopu
Konfokálna mikroskopia pomáha študovať schopnosť rôznych látok akumulovať sa v jadre, cytoplazme alebo iných bunkových štruktúrach. Tieto schopnosti sa často využívajú v procese výskumu mechanizmov účinku karcinogénov, protinádorových zlúčenín a liečiv a umožňujú tiež vypočítať ich efektívne koncentrácie.
Letálne štúdium intenzity, ako aj tvaru spektier vnútornej fluorescencie umožňuje rozpoznať zapálené a normálne bunky. Táto metóda sa používa v počiatočných štádiách diagnostiky rakoviny krčka maternice.
Správne zvolenú kombináciu rôznych filtrov navrhnutých pre niekoľko typov vnútornej fluorescencie je možné získať bez prácneho skúmania viacerých rezov. Týmto spôsobom sa dajú rýchlo a presne odhaliť a odlíšiť zhubné tkanivové štruktúry od normálnych.
Metódy konfokálnej mikroskopie sú široko používané v hydrobiológii a embryológii, botanike a zoológii v procese štúdia štruktúry gamét, ako aj vývoja a tvorby organizmov.
Konfokálne laserové mikroskopy v modernom svete našli široké uplatnenie v oblasti biológie, biofyziky, medicíny, bunkovej a molekulárnej biológie. Konfokálna mikroskopia je jedinečná bezkontaktná technika, ktorá sa dnes používa na štúdium rohovky oka. Umožňuje vám čo najpresnejšie posúdiť existujúci stupeň bunkových zmien a extracelulárnych štruktúr, ako aj vyvodiť závery o možnom poškodení rohovky ako celku.
Laserové konfokálne mikroskopy majú vysoké rozlíšenie, takže umožňujú študovať štruktúru fluorescenčne označených buniek a dokonca aj jednotlivé gény. Použitie rôznych technológií na špecifické viacfarebné fluorescenčné farbenie pre biologicky aktívne molekuly, ako aj supramolekulárne komplexy, umožňuje študovať komplexné mechanizmy fungovania nielen jednotlivých buniek, ale aj celých systémov. Táto technológia je široko používaná v experimentálnej biológii, ako aj v medicíne.
Vybavenie: konfokálne mikroskopy
Moderné ultra presné konfokálne mikroskopy, ako napríklad Leica TCS SP8, vám umožňujú získať najjasnejšie a najspoľahlivejšie údaje pri vykonávaní rôznych štúdií. Široký záujem o takéto zariadenia vznikol v osemdesiatych rokoch minulého storočia v dôsledku prudkého rozvoja výpočtovej techniky a laserových technológií.

Konfokálna laserová skenovacia mikroskopia je typ optickej mikroskopie. Jeho zvláštnosťou je, že laserový lúč je zaostrený na konkrétnu oblasť pozdĺž osi X a Y a vytvára tak obraz. Odrazené svetlo je zobrazené na obrazovke vo forme rastra. Veľkosť obrazu priamo závisí od rozlíšenia modernej elektroniky, ako aj od veľkosti naskenovaného rastra.
Meracie prístroje, ktoré boli vytvorené pomocou modernej metódy konfokálnej laserovej skenovacej mikroskopie, sa v súčasnosti rozšírili v rôznych oblastiach. V porovnaní s konvenčnou svetelnou mikroskopiou má konfokálna mikroskopia nasledujúce výhody:
- zlepšené rozlíšenie;
- vysoký kontrast obrazu;
- schopnosť vykonávať multispektrálne štúdie s vysokým stupňom separácie signálov;
- schopnosť získať „optické rezy“ pomocou trojrozmernej rekonštrukcie;
- možnosť využitia metód digitálneho spracovania získaných obrázkov;
Nevýhody opísaného zariadenia zahŕňajú:
- zložitosť nastavenia zariadenia;
- nedostatok optického obrazu;
- vysoké náklady na zariadenia, ako aj vysoké náklady na ich údržbu.
Konfokálny mikroskop využíva na ovládanie celého systému špeciálny počítač. Umožňuje ukladať obrázky a podrobne študovať výsledné údaje. Kvalitné spracovanie výsledných obrázkov si často vyžaduje pomerne veľký výpočtový výkon, takže počítač musí disponovať pomerne veľkou RAM. Pre ďalšie ukladanie informácií je potrebná aj veľká disková pamäť. Na prenos obrázkov musí mať takýto počítač port USB alebo disk CD/DVDRW. Počítač má tiež možnosť pripojenia na globálny internet alebo lokálnu sieť.
Softvér nainštalovaný na takýchto počítačoch môže byť základný. Dodáva sa s výbavou a umožňuje spravovať celý systém a sledovať jeho základné funkcie. Pre tieto počítače sú špeciálne vyvinuté aj balíčky aplikačných úloh, ktoré sa objednávajú dodatočne. Mnohé modely konfokálnych mikroskopov majú špeciálny ovládací panel, ktorý umožňuje konfigurovať ich činnosť na diaľku.
Nainštalujte opísané zariadenia počas bežných laboratórnych návštev. Najdôležitejším postupom pri prevádzke konfokálnych mikroskopov je kontrola vibrácií. Na tieto účely sa používa špeciálne zariadenie, ktoré meria úroveň vibrácií. Postup kontroly je podobný postupu merania axiálneho rozlíšenia LSCM pomocou zrkadla.
Konfokálna mikroskopia sa rýchlo rozvíja. Známe výrobné spoločnosti prezentujú na trhu najnovšie modely konfokálnych mikroskopov, ktoré umožňujú efektívne oddeliť laserový excitačný lúč, ako aj luminiscenciu. Rozdeľovač lúčov v takýchto zariadeniach je riadený počítačom. Jeho spektrálne vlastnosti je možné v prípade potreby rýchlo vyladiť na niekoľko laserových línií.
Konfokálne mikroskopy v mikrobiológii
Konfokálny mikroskop je tiež nevyhnutný v biológii na podrobné štúdium buniek. Dnes na túto tému vychádza obrovské množstvo rôznych vedeckých článkov. Najčastejšie sa konfokálne mikroskopy používajú na štúdium štruktúry buniek, ako aj ich organel. Študuje sa aj kolokalizácia v bunke, aby sa pochopilo, či medzi bunkovými substanciami existuje vzťah príčina-následok.
V procese štúdia proteínov konfokálnymi mikroskopmi sú predbežne označené protilátkami s rôznymi fluorochrómami. Pomocou bežného klasického mikroskopu je dosť ťažké rozoznať, či sú umiestnené vedľa seba alebo pod sebou, ale konfokálny mikroskop to bez problémov umožňuje. Údaje o sérii optických rezov sa zaznamenajú do pamäte počítača a tým sa vykoná objemová rekonštrukcia objektu a získa sa aj jeho trojrozmerný obraz.
Pomocou konfokálnych mikroskopov sa tiež študujú dynamické procesy prebiehajúce v živých bunkách, napríklad pohyb iónov vápnika alebo iných látok cez bunkové membrány. Konfokálne mikroskopy sa používajú aj na štúdium mobility bioorganických molekúl pomocou ionizácie fotochemického rozkladu fluorochrómu v ožarovacej zóne, ako aj jeho následnej disociácie z molekúl. Takéto molekuly sú označené dvoma fluorochrómami, ktoré majú emisné spektrum donoru, ktoré sa prekrýva s absorpčným spektrom akceptora. Energia sa teda prenáša z darcu na akceptor na krátke vzdialenosti a v dôsledku rezonancie medzi energetickými hladinami. Potom akceptor vyžaruje energiu vo viditeľnej oblasti spektra, ktorá sa následne zaznamená pomocou konfokálneho mikroskopu.
Vývoj konfokálnej mikroskopie pokračuje. Výrobcovia tohto zariadenia každoročne prezentujú na trhu stále modernejšie, funkčné a vylepšené mikroskopy, čo vedcom umožňuje robiť nové užitočné objavy v rôznych oblastiach. Vylepšuje sa aj softvér určený pre počítače, ktoré sú vybavené konfokálnymi mikroskopmi. Umožňuje vám realizovať najzložitejšie úlohy, ktoré umožňujú vykonávať výskum na molekulárnej a bunkovej úrovni. Dnes môžeme s istotou povedať, že konfokálne mikroskopy sú budúcnosťou, pretože svojimi funkčnými vlastnosťami a technickými možnosťami výrazne prekonali bežné mikroskopy. Medzi pomerne širokou škálou konfokálnych optických zariadení si každý používateľ bude môcť vybrať ten správny mikroskop pre seba, čo mu umožní aktívne rozvíjať svoj výskum.
Príbeh
V 50. rokoch potrebovali biológovia zvýšiť kontrast pozorovania predmetov označených fluorochrómom v rezoch hrubého tkaniva. Na vyriešenie tohto problému Marvin Minsky, profesor v USA, navrhol použiť konfokálnu schému pre fluorescenčné mikroskopy. V roku 1961 získal Minsky patent na túto schému.
Princíp činnosti
Konfokálny mikroskop má rovnaké rozlíšenie ako bežný mikroskop a je obmedzený difrakčným limitom.
kde je vlnová dĺžka žiarenia, je numerická apertúra šošovky, je index lomu média medzi vzorkou a šošovkou, je polovica uhla, ktorý šošovka „zachytí“. Vo viditeľnom rozsahu je rozlíšenie ~ 250 nm (NA=1,45, n=1,51).V posledných rokoch sa však úspešne vyvinuli návrhy mikroskopov, ktoré využívajú nelineárne vlastnosti fluorescencie vzoriek. V tomto prípade sa dosiahne rozlíšenie, ktoré je výrazne nižšie ako difrakčný limit a dosahuje ~ 3-10 nm.
Konfokálny mikroskop vytvára jasný obraz vzorky, ktorý by sa pri bežnom mikroskope javil rozmazaný. To sa dosiahne odrezaním svetla pozadia prichádzajúceho z hĺbky vzorky pomocou clony, to znamená svetla, ktoré nedopadá na ohniskovú rovinu šošovky mikroskopu. Výsledkom je obraz s lepším kontrastom ako bežný optický mikroskop.
Obrázok je dvojrozmerný (2D) obrázok.
pozri tiež
Výhody v biológii oproti iným mikroskopom
Index lomu biologických predmetov je takmer rovnaký ako u skla, takže pozorovanie týchto predmetov na povrchu podložného sklíčka je v bežnom mikroskope veľmi náročné. Konfokálny mikroskop, ktorý má vysoký kontrast, poskytuje dve neoceniteľné schopnosti: umožňuje študovať tkanivo na bunkovej úrovni v stave fyziologickej aktivity a tiež vyhodnocovať výsledky štúdie (to znamená bunkovú aktivitu) v štyroch dimenziách - výška, šírka, hĺbka a čas.
Poznámky
Odkazy
- Molekulové výrazy: Laserová skenovacia konfokálna mikroskopia
- Nikon's MicroscopyU. Komplexný úvod do konfokálnej mikroskopie.
- Emoryho fyzikálne oddelenie. Úvod do konfokálnej mikroskopie a fluorescencie.
- Prehľad konfokálnej mikroskopie časopisu Science Creative Quarterly – k dispozícii sú aj obrázky s vysokým rozlíšením.
- Programmable Array Microscope - Možnosti konfokálneho mikroskopu.
Nadácia Wikimedia. 2010.
Pozrite sa, čo je „konfokálny mikroskop“ v iných slovníkoch:
Tento výraz má iné významy, pozri Mikroskop (významy). Mikroskop, 1876 ... Wikipedia
Mikroskop atómovej sily Mikroskop atómovej sily (AFM atomic force microscope) je skenovací sondový mikroskop s vysokým rozlíšením. Používa sa na určenie topografie povrchu s rozlíšením z des... Wikipedia
Všeobecný názov pre metódy pozorovania objektov nerozoznateľných ľudským okom cez mikroskop. Ďalšie podrobnosti nájdete v čl. (pozri MIKROSKOP). Fyzický encyklopedický slovník. M.: Sovietska encyklopédia. Šéfredaktor A. M. Prochorov. 1983... Fyzická encyklopédia
- (anglicky: dusík vacancy center) alebo dusíkom substituovaná vakancia v diamante je jedným z mnohých bodových defektov v diamante. Defekt je porucha v štruktúre diamantovej kryštálovej mriežky, ku ktorej dochádza pri odstránení atómu... ... Wikipedia
Wikipedia obsahuje články o iných ľuďoch s týmto priezviskom, pozri Minsky. Wikipedia obsahuje články o iných ľuďoch s týmto priezviskom, pozri Minsky. Marvin Lee Minsky anglicky Marvin Lee Minsky ... Wikipedia
Minsky, Marvin Lee Americký vedec v oblasti umelej inteligencie Dátum narodenia: 9. august 1927 (19270809) ... Wikipedia
Minsky, Marvin Lee Americký vedec v oblasti umelej inteligencie Dátum narodenia: 9. august 1927 (19270809) ... Wikipedia
Minsky, Marvin Lee Americký vedec v oblasti umelej inteligencie Dátum narodenia: 9. august 1927 (19270809) ... Wikipedia
Lee americký vedec v oblasti umelej inteligencie Dátum narodenia: 9. august 1927 (19270809) ... Wikipedia
knihy
- Konfokálna mikroskopia a ultramikroskopia živej bunky, Georgy Michajlovič Svishchev. Konfokálny mikroskop je typ skenovacieho svetelného mikroskopu. Pri skúmaní hrubých predmetov vytvára obrázky bez pozadia, ktoré konvenčné mikroskopy vytvárajú...





Rad mobilných procesorov Intel Haswell Core 4. generácie
Stiahnite si rozšírenú verziu protanki modpack pre wot
Merač sobov od Jove pre WoT
Optimalizácia výkonu počítača Stiahnite si programy pre hru World of Tank
Rozhranie PCI-Express, jeho hlavné charakteristiky a spätná kompatibilita